Наш 37-Й СЛУЧАЙ МОДИФИЦИРОВАННОЙ ОПЕРАЦИИ APPLEBY оказался экзотическим. Это первое описание такого наблюдения, но, безусловно, мы возьмем этот опыт на вооружение. #ракТелаПоджелудочнойЖелезы
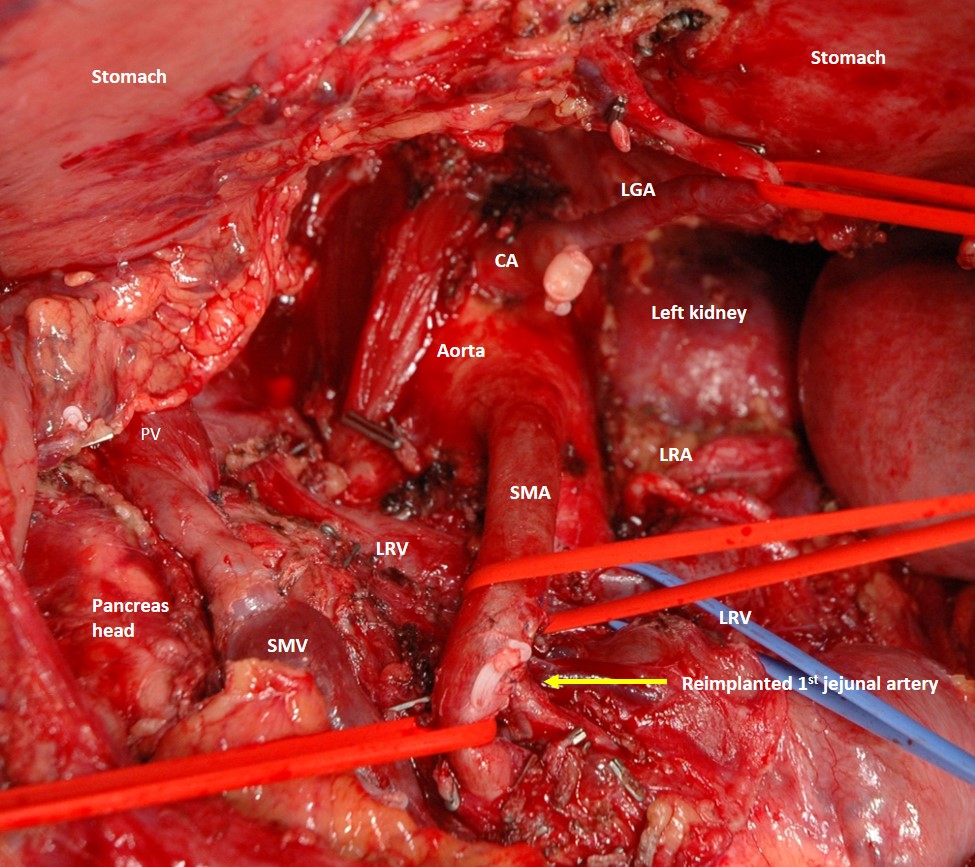
R0- дистальная резекция поджелудочной железы + Резекция чревного ствола (модифицированная операция #Aplleby) с сохранением левой желудочной артерии, резекция средней толстокишечной и первой тонкокишечной артерии с реплантацией последней в верхнюю брыжеечную. Резекция воротной вены. Спленэктомия. Левосторонняя адреналэктомия (posterior RAMPS). Расширенная лимфодиссекция (за счет удаления параортальных лимфоузлов). Холецистэктомия.
Семь курсов предоперационной химиотерапии: #протоковаяАденокарциномаПоджелудочнойЖелезы.
16 лет после передней резекции: #ракПрямойКишки (с промежуточной операцией по закрытию трансверзостомы) без рецидива.
R0 distal pancreatectomy with the celiac, middle hepatic and first intestinal arteries resection, preservation of the left gastric artery and replantation of the first intestinal artery into the superior mesenteric artery. PV/SMV resection. Splenectomy. Left adrenalectomy (posterior RAMPS). Cholecystectomy. Extended lymph node dissection (9,12th and 16th groups) Sixteen years after anterior resection for #rectalCancer (with the inferior mesenteric artery excision) and 3 weeks after 7 courses of the mFOLFIRINOX chemotherapy for PDAC.
Прошла неделя, как на 9-й день после вышеуказанной операции мы выписали 67-летнюю пациентку в отличном состоянии. Послеоперационный период протекал без осложнений с 3-го послеоперационного дня, но само вмешательство и первые два дня после нее были экзотическими.
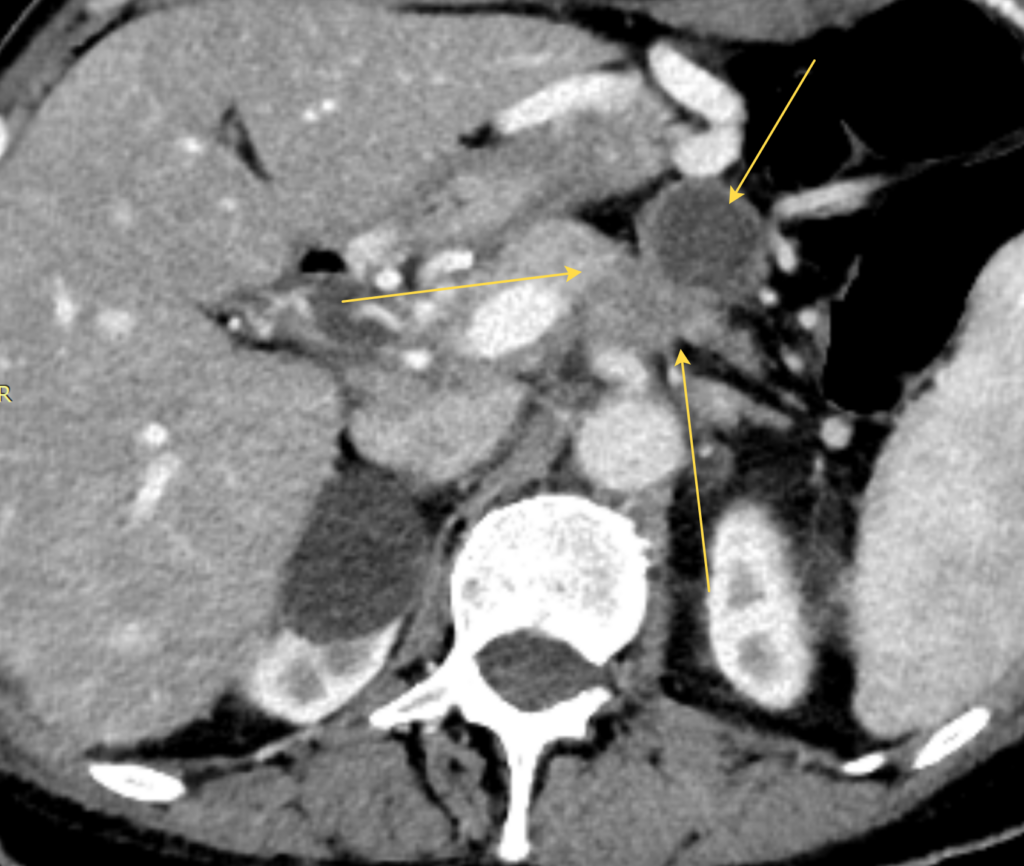
Около полугода назад у нашей больной появились боли в пояснице и верхних отделах живота. При КТ и МРТ был выявлен рак тела поджелудочной железы с вовлечением ветвей чревного ствола. Не без побочных эффектов пациентка прошла 7 курсов химиотерапии, на контрольных КТ и МРТ было выявлено отсутствие прогрессирования. Имея большой опыт таких операций (#DPCAR), мы предложили больной радикальную дистальную резекцию поджелудочной железы с резекцией чревного ствола. Необычной и серьезной проблемой было то, что по данным КТ было отмечено вовлечение в опухоль средней толстокишечной артерии (один из ключевых сосудов, кровоснабжающих толстую кишку после удаления нижней толстокишечной артерии), и тесное прилегание опухоли к 1-ой тонкокишечной артерии, от которой отходит нижняя панкреатодуоденальная — ключевая коллатераль для кровоснабжения печени при резекции чревного ствола.
Другими словами, радикальное удаление опухоли поджелудочной железы могло вызвать ишемию (дефицит артериального кровотока) печени и левой половины толстой кишки, для предотвращения которого могла потребоваться артериальная реконструкция общей печеночной и средней толстокишечной артерий. При резекциях (удалении части) поджелудочной железы артериальные реконструкции значительно повышают риск операций, т.к. в случае возникновения панкреатических фистул и воздействия панкреатического сока на область соединения артерий повышается риск арозивных кровотечений, которые нередко бывают смертельными. Из названия операции видно, что избежать артериальной реконструкции нам не удалось, она была сделана, но в экзотическом для этой хирургии области.
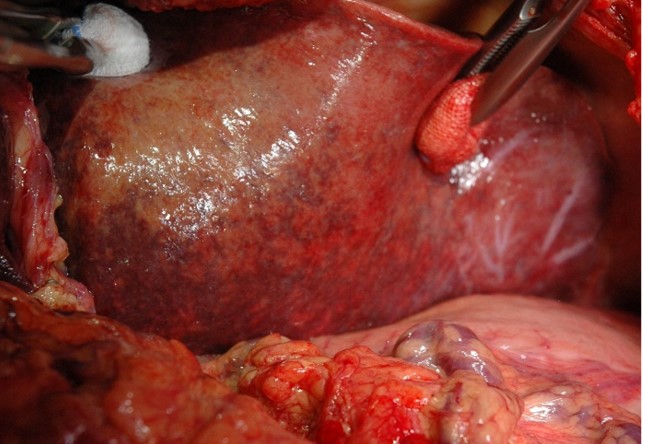
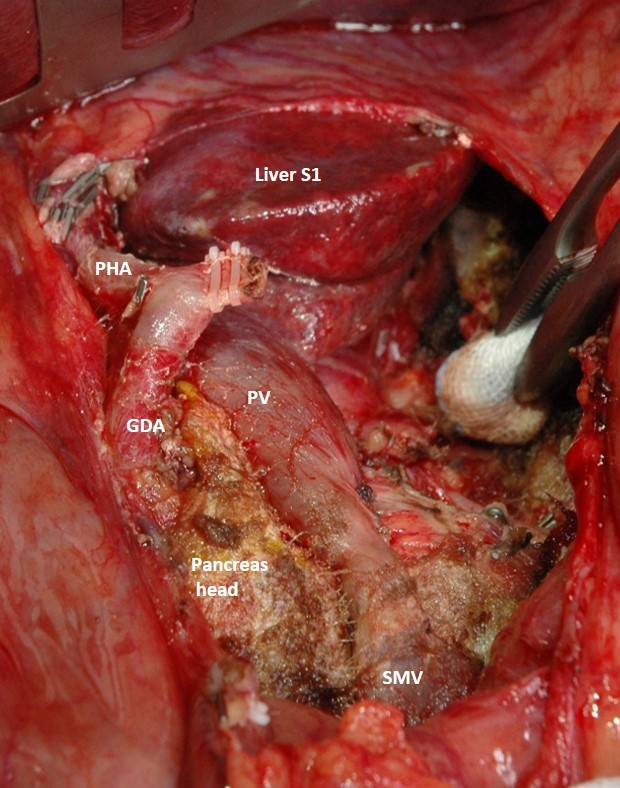
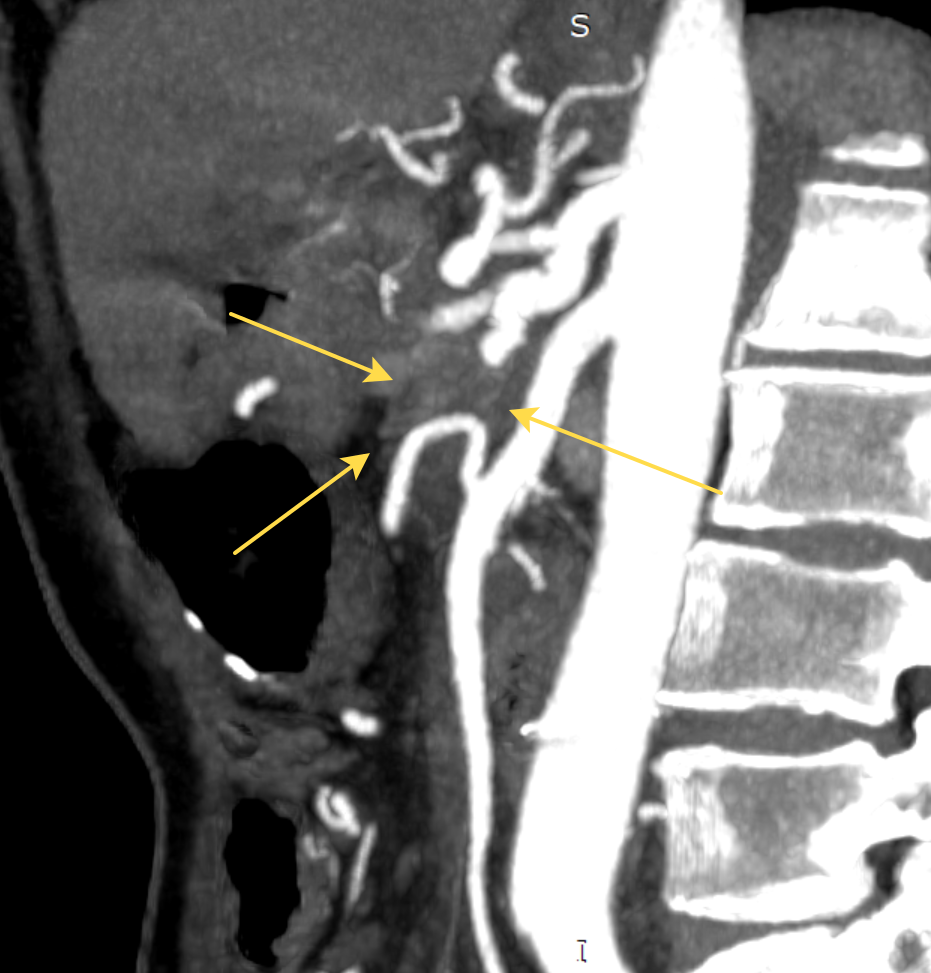
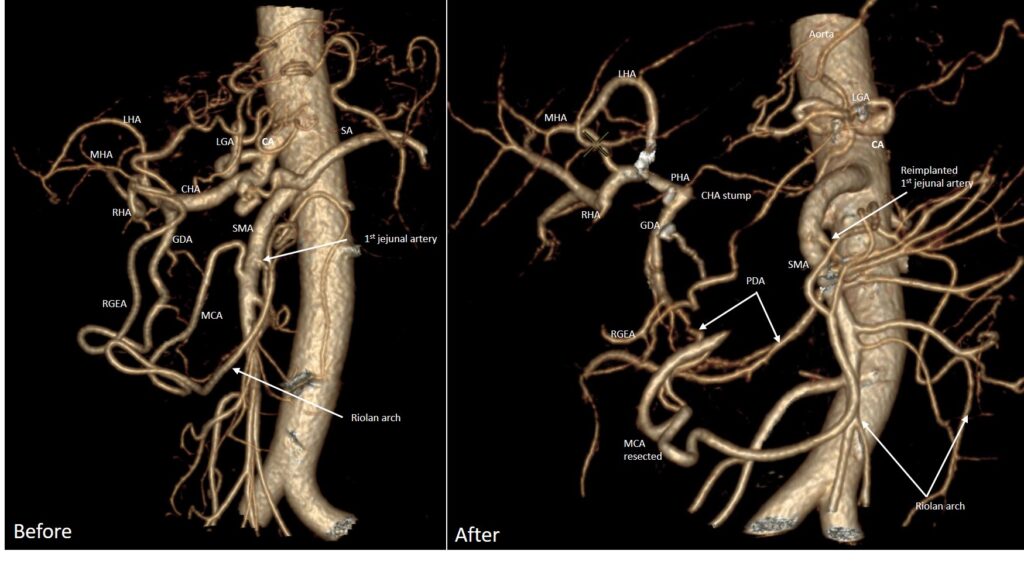
При этих вмешательствах для контроля за кровоснабжением органов (в первую очередь, желудка и печени) мы всегда используем динамический (т.е. часто повторяющийся интраоперационный УЗ (ИОУЗИ) и флюоресцентную артериографию с использованием ICG. При пережатии общей печеночной артерии (ОПА) на собственной печеночной (СПА) сохранился пульс, кровоток в печени сменился с магистрального на коллатеральный, но остался адекватным. При скелетировании верхней брыжеечной артерии (ВБА) была выделена средняя толстокишечная артерия (СТКА), ее пережатие не повлияло на пульсацию риолановой дуги толстой кишки, и она была резецирована (см КТ-ангиографию). При отделении опухоли от адвентиции первой тонкокишечной ветви возникло кровотечение, а ушивание микродефекта привело к сужению артерии. Это сужение оказалось значимым, т.к. при пережатой ОПА перестал определяться пульс на СПА и резко снизился артериальный кровоток в паренхиме печени. Тогда первая тонкокишечная ветвь была отсечена от ВБА, устье ее было расширено, и она была реимплантирована обратно в ВБА (Сослан Дзигасов). Пульс на ОПА и кровоток в печени восстановился. Мы выбрали такой путь вместо реконструкции ОПА для того, чтобы отнести зону артериальной реконструкции как можно дальше от среза поджелудочной железы, истечение сока из которого случается в 35-50% случаев после таких операций, когда линия среза проходит через головку ПЖ. Операция была завершена без происшествий, кровопотеря 400 сс, уровень резекции R0 (нет опухолевых клеток при микроскопии краев удаленного препарата, см. фото), левую желудочную артерию удалось сохранить, ИОУЗИ и флюоресцентная ангиография не показали нарушений кровоснабжения печени, желудка и толстой кишки, уровень лактата и трансаминаз мало отличался от нормы, несмотря на резекцию артерий и вены (сужение диаметра на 50%) с временным (25 мин и 4 мин) прекращением кровотока в них.
Однако, на этом нюансы не кончились. Довольно необычным, но ярким осложнением раннего послеоперационного периода стал редкий неврологический синдром – мутизм. Пациентка могла общаться невербально, отвечать, да и нет с помощью поворота головы. Была в хорошем настроении, у нее ничего не болело, но она не разговаривала. Это нас очень удивило и встревожило, после исключение острых неврологических событий, стали думать в чем причина. Основной нашей гипотезой мы выбрали развитие мутизма как редкого осложнения тотальной внутривенной анестезии или действие субгипнотических доз кетамина (с целью анальгезии и профилактики гипералгезии) на фоне сниженной функции печени. Возможный вариант – центральный антихолинэргический синдром, но мутизм как элемент диссоциации на фоне кетамина и сниженной печеночной функции, нам показался более вероятным. В нашем случае повреждение печени могло быть комбинированным, вследствие стеатогепатита (CASH), от воздействия 5-FU и иринотекана и SOS (toxic sinusoidal injury, veno-occlusive disease or «blue liver syndrome»), вследствие воздействия оксалиплатина. В литературе описано несколько таких случаев (https://journals.lww.com/anesthesia-analgesia/Fulltext/2003/01000/An_Unusual_Complication_of_Total_Intravenous.35.aspx), в некоторых из них мутизм длился до 11 дней, к счастью для нас и пациентки, через 24 часа она заговорила, и в дальнейшем, послеоперационный период протекал без осложнений.
Это сложная и слаженная работа онкологической, хирургической, анестезиологической, реаниматологической, реабилитационной, психотерапевтической команд нашей больницы, без которых такие уникальные вещи невозможны.